-
-
پيوندها
- فروش ساعت مچی" title="" target="_blank" >فروش ساعت مچی
- مرجع فناوری و تکنولوژی(نارنجی)
- سایت تخصصی علوم تجربی
- اپراتور رایتل
- وبسایت شخصی مهندس ساکت
- فیزیک
- ردیاب ماشین
- جلوپنجره اریو
- اریو زوتی z300
- جلو پنجره ایکس 60
- قالب رز بلاگ
-
آرشيو
-
پيوندهاي روزانه
-
آخرين نوشته هاي من
- ناپلئون بناپارت
- لویی شانزدهم
- عکس هایی از ایسلند
- با پاریس اشنا شوید
- اندام تناسلی زن
- سیستم ادراری
- لویی پاستور
- مکانیک کوانتوم
- برو به ادامه مطلب
- نظریه اشوب
- اینتل از ویلچر هوشمد خود برای استیون هاوکینگ پرده برداشت
- اطلاعاتی در مورد ابراهام لینکلن
- لوئی دوازدهم
- بیایید ایزاک اسیموف را کمی بهتر بشناسیم.
- فرانسیس بیکن که بود؟
- مطالبی در مورد بیوشیمی
- زیست سلولی و مولکولی چیست؟؟؟؟؟؟؟؟؟
- بافت ابکش
- آلانین آمینوترانسفراز
پربازديدترين ها
- الت تناسلی مرد چیست؟
- پرچم در گل چیست؟
- ماشین های تورینگ
- مکتب فیثاغورثیان
- امیلاز چیست؟
- نقد و بررسی نوکیا دویست و شش
- کتب ریاضی
- عصر رنسانس
- هورمون انژیوتانسین چیست؟
- هندسه تحلیلی چیست؟
- جابر ابن حیان
- حسابان
- هندسه2
- قرون وسطی
- اسپرم
- منظومه شمسی
- فئودالیسم
- زبان المانی
- رنسانس 2
- تار (ساز)
- اقتصاد
- زمین شناسی چیست؟
- علم ترکیبیات
- فیودور داستایوسکی که بود؟
- برنامه نویسی
- طلا
- خون
- ژایگاه داده چیست؟
- هورون اکسی توسین چیست؟
- عدد جبری
- منطق فازی
- نقد و بررسی نکسوس 10
- نقد و بررسی نوکیا لومیا نهصد و بیست و پنچ(طرح نقد و بررسی موبایل)
- مطلبی در مورد انقلاب کبیر فرانسه
- ترکیبات کووالانسی
- معرفی چند کتاب ریاضی
- نقد وبررسی نوکیا اشا سیصد و پنج(طرح معرفی موبایل)
- نجوم رصدی
- دستگاه عصبی
- برای نجومی ها
- پیوند هیدروژنی
- شرکت ال جی
- زیست سلولی و مولکولی چیست؟؟؟؟؟؟؟؟؟
- نقد وبررسی نوکیا لومیا نهصد وبیست(طرح معرفی موبایل)
- جنگ جهانی دوم
- دانشمند ریاضی
- ترکیب گزاره های ریاضی 1
- پارادوکس
- ژاپن
- معرفی بعضی از دانشمندان شیمی
مطالب تصادفی
- در مورد رادیو اکتیو
- هندسه
- پارادوکس
- algorithm
- کتب ریاضی
- هندسه3
- برنامه نویسی
- معرفی وبلاگ
- معرفی بعضی از دانشمندان شیمی
- بلکین و عرضه کیس-کیبرد پرتابل ویژه آیپد مینی
- ژاپن
- سالگرد تولد وبلاگ مقاله های علمی . تخصصی
- اپل نام ایران را از فهرست کشورهای «تحت تحریم کامل» خود خارج ساخته است
- نقد و بررسی نوکیا لومیا ششصد و بیست
- سونی اکسپریا i1 با اندامی باریک در تصویر لو رفته ظاهر شد
-
موضوعات وبلاگ
- تایپک کامپیوتر
- مبانی کامپیوتر تعداد پست ها: 7
- برنامه نویسی تعداد پست ها: 1
- تبلت.اولترابوک.نوت بوک تعداد پست ها: 19
- تاریخچه کامپیوتر ها تعداد پست ها: 5
- تایپک علوم تجربی
- فیزیک تعداد پست ها: 17
- شیمی تعداد پست ها: 15
- زیست شناسی تعداد پست ها: 33
- زمین شناسی تعداد پست ها: 3
- تایپک اختر شناسی و نجوم
- تایپک ریاضی
- هندسه تعداد پست ها: 10
- جبر و انالیز تعداد پست ها: 11
- منطق تعداد پست ها: 13
- کتب ریاضی تعداد پست ها: 5
- علوم اجتمایی
- تاریخ تعداد پست ها: 21
- جغرافیا تعداد پست ها: 6
- اقتصاد تعداد پست ها: 4
- فلسفه و الهیات
- موسیقی
- کلاسیک تعداد پست ها: 0
- سنتی تعداد پست ها: 2
- معرفی ساز ها تعداد پست ها: 3
-
-
-
امکانات وبلاگ
وب : پیام : 2+2=: (Refresh)  خبرنامه وب سایت:
خبرنامه وب سایت:
 آمار
وب سایت:
آمار
وب سایت:
بازدید امروز : 1
بازدید دیروز : 5
بازدید هفته : 68
بازدید ماه : 63
بازدید کل : 90207
تعداد مطالب : 178
تعداد نظرات : 11
تعداد آنلاین : 1 -
طراح قالب: NEGASH.IR
ارائه کننده متفاوت ترين قالب ها براي سرويس هاي وبلاگدهي فارسي
-
درباره من
با سلام. من محمد حسن ابوالحسنی هستم.من دانش اموز سمپاد هستم و به وبلاگنویسی علاقه دارم.موضوعات کلی این وبلاگ شامل علوم پایه و نجوم و علوم اجتماعی و .. است.امید وارم از این وبلاگ خوشتان بیاید.
پروفايل من -
آخرین ارسال های انجمن
عنوان پاسخ بازدید توسط ForumPostCountAnswer [ForumPostLastAuthor] [] [loxblog] نويسنده: [cb:post_author_name] | [cb:post_create_date] ساعت [cb:post_create_time]
پیوند هیدروژنیعلوم طبیعت > شیمی > شیمی معدنی
هرگاه هیدروژن به اتمی با الکترونگاتیوی زیاد مثل فلوئور ، اکسیژن یا نیتروژن متصل گردد، شرایطی برای بوجود آمدن نوع بسیاری مهمی جاذبه بین مولکولی مثبت ـ منفی که آن را پیوند هیدروژنی میگویند حاصل میشود. به عبارت دیگر ، اتم هیدروژن یک مولکول و زوج الکترون غیر مشترک مولکول دیگر متقابلا همدیگر را جذب میکنند و پیوندی تشکیل میشود که به پیوند هیدروژنی ، Hydrogen Bond مرسوم است.
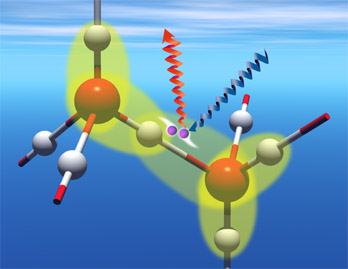
اطلاعات اولیه
دربرخی از
بطور غیرعادی قوی است. این جاذبه در ترکیباتی مشاهده میشود که درآنها بین هیدروژن و
که اندازه کوچک و
زیاد دارند، پیوند هیدروژنی وجود دارد. پیوند هیدروژنی نه تنها بین مولکولهای یک نوع ماده ، بلکه بین مولکولهای دو ماده متفاوت که توانایی تشکیل پیوند هیدروژنی را دارند نیز برقرار میشود.
نحوه تشکیل پیوند هیدروژنی
پیوند هیدروژنی بر اثر جاذبه اتم هیدروژن اندک مثبت موجود در یک مولکول و اتم بسیار الکترونگاتیو
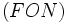
موجود در مولکول دیگر (یا در محل دیگر همان مولکول اگر مولکول به قدر کافی بزرگ باشد که بتواند روی خود خم شود) تولید میگردد. جا به جا شدن یک
به سمت عنصر بسیار الکترونگاتیو نیتروژن ، اکسیژن یا فلوئور موجب میشود که این اتمها دارای بار منفی جزئی شوند.
در این صورت پیوند هیدروژنی پلی است میان دو
شدیدا الکترونگاتیو با یک اتم هیدروژن که از طرفی بطور
با یکی از اتمهای الکترونگاتیو و از طرف دیگر بطور
(جاذبه مثبت به منفی) با اتم الکترونگاتیو دیگر پیوند یافته است. استحکام پیوند هیدروژنی
یکدهم
تا
یکپنجاهم
قدرت یک
متوسط است.
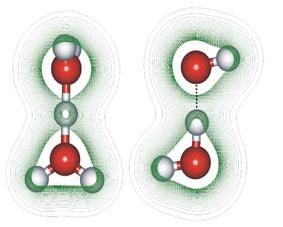
شرایط تشکیل پیوند هیدروژنی
- بالا بودن الکترونگاتیوی اتمهای متصل به هیدروژن: برهمین اساس است که فلوئور (الکترونگاتیوترین عنصر) ، قویترین پیوند هیدروژنی و اکسیژن (الکترونگاتیوتر از نیتروژن) ، پیوند هیدروژنی قویتری درمقایسه با نیتروژن تشکیل میدهد. همچنین بار مثبت زیاد بر روی اتم هیدروژن ، زوج الکترون مولکول دیگر را بشدت جذب میکند و کوچک بودن اندازه اتم هیدروژن سبب میشود که ملکول دوم بتواند به آن نزدیک شود.
- کوچک بودن اتمهای متصل به هیدروژن : پیوند هیدروژنی واقعا مؤثر فقط در ترکیبات فلوئور ، اکسیژن و نیتروژن تشکیل میشود. با وجود اینکه دو اتم نیتروژن و کلر ، الکترونگاتیوی برابر دارند، چون اتم کلر از اتم نیتروژن بزرگتر است بر خلاف نیتروژن ، کلر پیوند هیدروژنی ضعیفی تشکیل میدهد.
توجیه خواص غیرعادی برخی از مواد
وجود خواص غیرعادی برخی از مواد در حالت
یا
از جمله بالا بودن دماهای ذوب و جوش ، نشان میدهد که نیروهای جاذبه بین مولکولی در آنها به اندازهای زیاد است که نمیتوان آن را به تأثیرهای متقابل ضعیف بین مولکولی نسبت داد. آشناترین این نوع مواد ، فلوئورید هیدروژن ، آب و آمونیاک است که بسیاری از خواص آنها از جمله دماهای جوش و ذوب آنها از دماهای جوش و ذوب ترکیبهای مشابه خود ، برای مثال
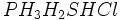
بطور غیرمنتظرهای بالاتر است.
شاید تصور شود که علت این وضعیت غیر عادی ، قطبیت به نسبت زیاد این مولکولهاست. البته تا اندازهای همین طور است. اما بررسی دقیق این پدیده غیر عادی نشان میدهد که باید نیروی جاذبه قویتر از نیروهای جاذبه دوقطبی _ دوقطبی بین مولکولهای آنها برقرار باشد.
اگر به ساختار الکترونی مولکولهای
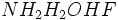
توجه شود، میتوان به موردهای مشترک بین آنها پی برد. این وجه اشتراک ، وجود دست کم یک پیوند کوالانسی با اتم هیدروژن و یک
دو الکترونی اتم مرکزی بسیار الکترونگاتیو در هر یک از آنهاست.
اتمهای
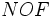
الکترونگاتیوی بالایی دارند با هیدروژن پیوند کوالانسی بشدت قطبی بوجود میآورند، بطوری که هیدروژن به میزان قابل توجهی خصلت یک
را پیدا میکند. جفت الکترون ناپیوندی و قابل واگذاری روی اتم الکترونگاتیو H ، این امکان را پدید میآورد که اتم هیدروژن در نقش پل ، اتمهای الکترونگاتیو دو
را به یکدیگر متصل کند و نیروی جاذبه بین مولکولی بوجود میآید که به پیوند هیدروژنی مرسوم است.
خواص ترکیبات دارای پیوند کووالانسی
ترکیباتی که مولکولهای آنها از طریق پیوند هیدروژنی به همدیگر پیوستهاند، علاوه بر دارا بودن
بالا ، بطور غیرعادی در دمای بالا
میشوند و
،
و
آنها زیاد است.
علت شناور بودن یخ
روی آب شناور میماند، زیرا به هنگام
، منبسط میشود. سبب این انبساط پیوند هیدروژنی میان مولکولهای خمیده آب است ساختار خمیده یا زاویهای مولکول آب ناشی از آرایش چهار وجهی چهار جفت الکترون در
یک اتم است. ساختار زاویهای
و پیوند هیدروژنی میان مولکولهای آب به آن معنی است که هر مولکول آب میتواند حداکثر با چهار مولکول آب دیگر پیوند هیدروژنی داشته باشد.
پس آب مایع را میتوان به صورت خوشههایی از مولکولهای آب تصورکرد، خوشههایی که با پیوند هیدروژنی از مولکولهای آب ساخته شدهاند و دائم در حال حرکتند. شمار مولکولها در هر خوشه و سرعت حرکت خوشهها به
بستگی دارد. با سرد شدن آب ، مجموعههایی از مولکولهای آب که بسرعت در حرکتاند، کند میشوند و در نقطه انجماد به یکدیگر قلاب شده ساختمان سه بعدی منبسط شدهای را بوجود میآورند. این ساختمان گستردهتر موجب میشود که تراکم یخ کمتر از آب باشد.
ذوب شدن یخ در حدود 15% انرژی پیوندهای هیدروژنی را میشکند و این امر سبب فرو ریختن ساختار میشود. در نتیجه مایعی متراکم حاصل می گردد.
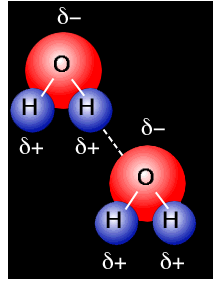
چرا نقطه جوش آب بالا است؟
خاصیت عجیب دیگر آب ، نقطه جوش نسبتا زیاد آن است. تقریبا تمام ترکیبات هیدروژندار مجاور اکسیژن و اعضای خانواده آن یعنی
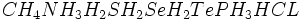
در دمای اتاق به حالت گازی هستند. اما آب مایع است. برای آنکه یک مولکول به حالت
در آید، باید انرژی جذب کند تا بتواند خود را از قید مولکولهای دیگر آزاد کند. چون آب مایع با پیوند هیدروژنی به صورت خوشههایی از مولکولها در میآید، برای شکسته شدن پیوندهای هیدروژنی آن ، انرژی زیادی لازم است.
اما همه پیوندهای هیدروژنی شکسته نمیشوند و خوشههایی از مولکولهای آب حتی در نزدیکی 1000 درجه سانتیگراد هنوز وجود دارند. وقتی آب گرم میشود، آشفتگی گرمایی پیوند هیدروژنی را میگسلد تا آنکه در
، فقط جزء کوچکی از شمار پیوندهای هیدروژنی موجود در آب مایع یا جامد باقی میماند. اگر پیوند محکم میان مولکولی از قبیل پیوند هیدروژنی وجود نداشته باشد، مواد معمولا بنا به
خود به جوش میآیند.
جرمهای مولکولی بزرگتر برای جوش آمدن به دمای زیادتری نیازمندند. عمدتا به این دلیل که
بزرگتر آسانتر و پیچیده میشوند و این امر ، منجر به
بین مولکولی قویتر میشود.
کاربردهای پیوند هیدروژنی
پیوندهای هیدروژنی در بسیاری از مواد یافت میشوند. پدیدههایی از قبیل چسبناک شدن آبنبات سفت ، دیرتر خشک شدن الیاف
از الیاف
، نرم شدن
با نایلون ، ناهنجارهای ظاهری در ماهیت آب ، همگی ناشی از همین پیوندهای هیدروژنی است.
موضوع : تایپک علوم تجربی , فیزیک , شیمی , زیست شناسی , ,
امتیاز : نتیجه : امتیاز توسط نفر مجموع امتیاز :
برچسب ها : پیوند هیدروژنی , پیوند کوالانسی , هیدروژن ,
بازدید : 2167
- بالا بودن الکترونگاتیوی اتمهای متصل به هیدروژن: برهمین اساس است که فلوئور (الکترونگاتیوترین عنصر) ، قویترین پیوند هیدروژنی و اکسیژن (الکترونگاتیوتر از نیتروژن) ، پیوند هیدروژنی قویتری درمقایسه با نیتروژن تشکیل میدهد. همچنین بار مثبت زیاد بر روی اتم هیدروژن ، زوج الکترون مولکول دیگر را بشدت جذب میکند و کوچک بودن اندازه اتم هیدروژن سبب میشود که ملکول دوم بتواند به آن نزدیک شود.

